Fisiopatologia delle lesioni muscolari

Fisiopatologia delle lesioni muscolari dalla classificazione alle fasi di rigenerazione delle lesioni e la fase di riabilitazione
Gli infortuni muscolari sono tra i più comuni infortuni che accadono nello sport con una frequenza che varia dal 10% al 55% di tutti quelli subiti [1-2].
Quasi tutti gli infortuni sembrano coinvolgere solo 4 gruppi muscolari: hamstring, adduttori, quadricipiti e muscoli del polpaccio [1].
Lesioni muscolari sono di tipo da rottura oppure necrosi in situ
Gli infortuni possono essere di tipo da rottura (causato da contusione, stiramenti o lacerazione), in cui le fibre muscolari, la loro lamina basale, le guaine, nonché i capillari vicini, si rompono tutti [2-3], oppure nell’altro tipo di lesione, necrosi in situ (o rabdomiolisi), le miofibrille sono parzialmente necrotizzate mentre la lamina basale, le guaine e i vasi sanguigni adiacenti rimangono intatti [2].
Oltre il 90% di tutti gli infortuni sportivi sono contusioni o stiramenti, mentre le lacerazioni muscolari sono lesioni non comuni negli sport [3]. La contusione muscolare si verifica quando un muscolo è sottoposto a una forza di compressione estrinseca, pesante e improvvisa, come un colpo diretto, cioè la lesione muscolare non è una conseguenza della forza intrinseca dell’esercizio stesso.
Negli stiramenti, le miofibrille sono esposte a una forza di trazione intrinseca eccessiva. La loro gravità varia da lesioni da sforzo molto lievi come la sindrome da indolenzimento muscolare a insorgenza ritardata (DOMS) a stiramenti “reali”, strappi da rottura, in cui le miofibrille e le strutture del tessuto connettivo associate, compresi i vasi sanguigni, si rompono [4].
I “veri” stiramenti muscolari indotti dall’esercitazione non differiscono in modo significativo nella loro risposta rigenerativa da quelli da contusioni o lacerazioni [5].
Patobiologia delle lesioni muscolari
Negli stiramenti, le miofibrille sono esposte a una tale forza di trazione intrinseca eccessiva che si verifica una ferita da lesione completa, cioè non solo la rottura delle miofibrille, ma anche della loro lamina basale, delle guaine e dei vasi sanguigni nell’endomisio o nel perimisio [3].
La rottura si trova più comunemente vicino alla giunzione miotendinea (MTJ). Questo punto spesso non è situato vicino ai tendini, dal momento che i muscoli si assottigliano verso i tendini stessi, numerose giunzioni si formano all’interno del ventre del muscolo, dove le miofibrille si attaccano alla fascia intramuscolare all’interno e intorno al muscolo.
Lesione muscolare: rigenerazione
La guarigione di una lesione da sforzo segue uno schema abbastanza costante, che è simile anche nelle contusioni o lacerazioni [3].
Questo processo è costituito da 3 fasi [2-3] (Fig. 1):
- Fase di distruzione
- Fase di riparazione
- Fase di rimodellamento
Nella fase di distruzione la miofibrilla rotta si necrotizza solo su un breve tratto. La propagazione della necrosi è fermata da una “porta del fuoco”, una fascia di contrazione formata entro un paio d’ore, che crea un’azione di sigillatura tramite un nuovo sarcolemma e lo spazio tra i monconi viene riempito da un ematoma. La lesione induce una reazione cellulare infiammatoria importante.
La fase di riparazione inizia con la fagocitosi del tessuto necrotizzato da parte di monociti derivati dal sangue. Le cellule di riserva miogeniche, le cellule satelliti, vengono attivate e iniziano la riparazione della miofibrilla lesionata. In primo luogo, le cosiddette cellule satellite dedicate iniziano a differenziarsi in mioblasti [6]. In secondo luogo, le cellule satellite staminali indifferenziate iniziano a proliferare nelle 24 ore e successivamente contribuiscono alla formazione di mioblasti, fornendo allo stesso tempo nuove cellule satellite, per divisione cellulare asimmetrica, al fine di sopperire a esigenze future di rigenerazione [6 -7].
I mioblasti derivanti dalle cellule satelliti dedicate e le staminali si fondono quindi per formare miotubi entro un paio di giorni [6]. Entro 5-6 giorni la parte necrotizzata della miofibrilla lesionata all’interno della vecchia lamina basale rimanente viene sostituita dalla rigenerazione di miofibrille, che quindi iniziano a penetrare nel tessuto connettivo della cicatrice tra i monconi delle miofibrille rotte. Anche il sito della lesione viene rivascolarizzato da capillari. I primi capillari angiogenici si osservano tre giorni dopo l’infortunio [8].
La fase di rimodellamento è il periodo di maturazione delle miofibrille rigenerate, che include la formazione di un apparato contrattile maturo e l’attacco delle estremità delle miofibrille rigenerate alla cicatrice interposta tra le giunzioni mio-tendinee appena formate.
La retrazione della cicatrice attira le estremità più vicine l’una all’altra, ma sembrano rimanere separate da un sottile strato di tessuto connettivo al quale le estremità rimangono attaccate tramite le giunzioni mio-tendinee appena formate [3].
La contrazione della grande granulazione nel tessuto cicatriziale è guidata dai fibroblasti che si trasformano in miofibroblasti capaci di effettuare la contrazione [9].
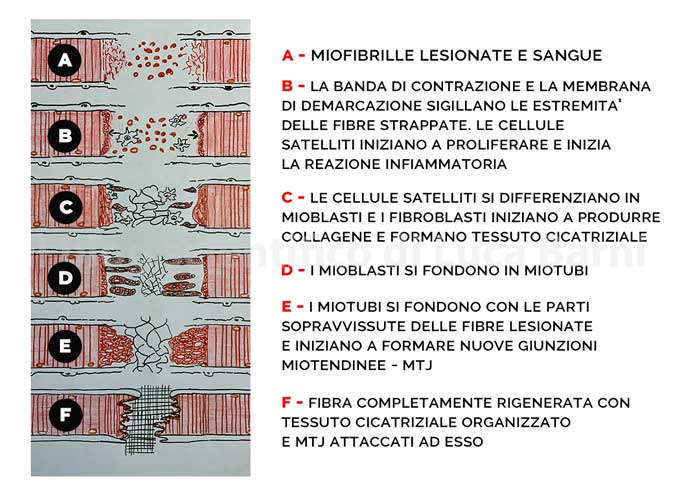
Fig. 1
Fisiopatologia lesioni muscolari: immobilizzazione e riabilitazione
Un breve periodo di inattività fisica completa (eseguita sotto forma di immobilizzazione) in seguito a un tipo di infortunio muscolare da lesione è obbligatorio e utile sia per la ripresa rapida che per il recupero completo. L’immobilizzazione consente al tessuto connettivo formato (tessuto di granulazione) di collegare tra loro i monconi muscolari danneggiati per ottenere la forza necessaria a resistere alle forze indotte dalle contrazioni applicate sul tessuto che si sta rigenerando senza provocare una ri-rottura.
Tuttavia, l’immobilizzazione deve essere limitata a durare meno di una settimana, in modo che gli effetti avversi dell’immobilità di per sé siano limitati al minimo [3-8-10]. Le ri-rotture nel sito del trauma muscolare originale cosi come il tessuto cicatriziale permanente di grandi dimensioni sono comuni se la mobilizzazione attiva viene iniziata immediatamente dopo l’infortunio [10]. Mettendo il muscolo lesionato a riposo per i primi 4-6 giorni dopo l’infortunio, è possibile prevenire l’eccessiva formazione di cicatrici e la ri-rotture nel sito che aveva subito la lesione [3,-8-10].
Evitare le ri-rotture è importante, poiché è stato dimostrato che le ri-rotture sono in realtà le lesioni del muscolo scheletrico più gravi che causano la più lunga assenza dall’attività sportiva [11].
L’immobilizzazione iniziale deve essere seguita da una riabilitazione attiva.
Una precoce mobilizzazione come trattamento primario del trauma muscolare fu inizialmente raccomandata, su indicazione in gran parte basata sulla sua vasta esperienza personale nella medicina dello sport del dr. Woodard nel 1953 [12].
Oggi questa nozione empirica è supportata da una considerevole quantità di prove sperimentali [3-8-13].
Pertanto, la mobilizzazione del muscolo scheletrico lesionato deve essere iniziata gradualmente (cioè entro i limiti del dolore) il più presto possibile, poiché la mobilizzazione precoce ha dimostrato di accelerare e intensificare la fase di rigenerazione delle fibre muscolari scheletriche lesionate così come indurre l’angiogenesi e l’afflusso di sangue alla zona lesa.
L’esercizio è anche cruciale per la rigenerazione a livello molecolare quantificata con l’induzione di molecole appropriate per la rigenerazione e il corretto orientamento delle miofibrille in fase di rigenerazione [3-8-13].
L’esame clinico deve essere effettuato immediatamente dopo il trauma a 1-3 giorni dall’evento traumatico, a quel punto le modalità di imaging (risonanza magnetica o ecografia) possono fornire utili approfondimenti sulla gravità della lesione e fornire una prima classificazione.
Durante i primi giorni dopo l’infortunio, un breve periodo di immobilizzazione accelera la formazione di tessuto di granulazione nel sito di lesione, ma si deve notare che la durata dell’attività ridotta (immobilizzazione) dovrebbe essere limitata solo fino a che la cicatrice non raggiunge una forza sufficiente per sopportare le forze di trazione indotte dalla contrazione muscolare senza rischi di ri-rottura [5].
A questo punto, dovrebbe essere avviata una graduale mobilizzazione seguita da un programma di esercizi progressivamente più intenso per ottimizzare la guarigione ripristinando la forza del muscolo danneggiato, prevenendo l’atrofia muscolare e la diminuzione di estensibilità, fattori che possono tutti essere causa di un’immobilizzazione prolungata [5].
Sulla base delle attuali conoscenze, il programma di riabilitazione dovrebbe consistere in esercizi di agilità progressiva e di stabilizzazione del tronco, nonché su esercizi personalizzati per rafforzare e allungare (esercizi eccentrici) il muscolo scheletrico che ha subito l’infortunio [14].
References
- Ekstrand J, Hägglund M, Waldén M. Epidemiology of muscle injuries in professional football (soccer). Am J Sports Med 2011; 39:1226-1232.
- Kalimo H, Rantanen J, Järvinen M. Muscle injuries in sports. Baillière’s Clinical Orthop 1997;2:1-24.
- Järvinen TAH, Järvinen TLN, Kääriäinen M, Kalimo H, Järvi- nen M. Biology of muscle trauma. Am J Sports Med 2005; 33:745-766.
- Äärimaa V, Rantanen J, Best T, Schultz E, Corr D, Kalimo H. Mild eccentric stretch injury in skeletal muscle causes transient effects on tensile load and cell proliferation. Scand. J Med Sci Sports 2004;14:367-372.
- Järvinen TA, Järvinen M, Kalimo H. Regeneration of injured skeletal muscle after the injury.
Muscles Ligaments Tendons J. 2014 Feb 24;3(4):337-45.
- Rantanen J, Hurme T, Lukka R, Heino J, Kalimo H. Satellite cell proliferation and expression of myogenin and desmin in re- generating skeletal muscle: evidence for two different popula- tions of satellite cells. Lab Invest 1995;72:341-347.
- Kuang S, Kuroda K, Le Grand F, Rudnicki MA. Asymmetric self-renewal and commitment of satellite stem cells in muscle. Cell 2007;129:999-1010.
- Järvinen M. Healing of a crush injury in rat striated muscle. 3. A microangiographical study of the effect of early mobilization and immobilization on capillary ingrowth. Acta Pathol Microbi- ol Scand 1976;84A:85-94
- Huard J, Li Y, Fu FH. Muscle injuries and repair: current trends in research. Journal of Bone & Joint Surgery 2002;84-A:822- 832.
- Järvinen M. Healing of a crush injury in rat striated muscle. 4. Effect of early mobilization and immobilization on the tensile properties of gastrocnemius muscle. Acta Chir Scand 1976;142:47-56.
- Brooks JHM, Fuller CW, Kemp SPT, Reddin DB. Incidence, risk and prevention of hamstring muscle injuries in profession- al rugby union. Am J Sports Med 2006;34:1297-1306.
- Kujala UM, Orava S, Järvinen M. Hamstring injuries: Current trends in treatment and prevention. Sports Med 1997;23:397- 404.
- Kannus P , Parkkari J, Järvinen TLN, Järvinen T AH, Järvinen M. Basic science and clinical studies coincide: active approach is needed in the treatment of sports injuries. Scand J Med Sci Sports 2003;13:150-154.
- Askling C, Tengvar M, Thorstensson A. Acute hamstring in- juries in Swedish elite football: a prospective randomized con- trolled clinical trial comparing two rehabilitation protocols. Br J Sports Med 2013;47:953-959.

salve il 6/4/2019 giocando a calcio ho avuto uno strappo ai muscoli ischiocrurali della coscia sinistra.questo è il referto della risonanza magnetica:
L’indagine eseguita con tecnica multiecho secondo i vari piani ha fatto apprezzare :
– marcata severa disomogeneità , come per lesione (totale/subtotale) , in
corrispondenza dell’inserzione sulla tuberosità ischiatica del mm. semitendinoso ,
semimembranoso e bicipite femorale con importante raccolta fluida corpuscolata
circostante oblunga ed estesa caudalmente al III medio di coscia , con severo
evidente impegno reattivo intra ed intermuscolare ; imbibizione edematosa del
tessuto cellulo-adiposo del III prossimale di coscia;
– segni di idrocele bilaterale.
In accordo con il medico curante si propone monitoraggio con u.s. ed RM a 30 gg.
volevo un vostro parere su questa lesione.la mia età è di 59 anni.
dopo 30 giorni ho rifatto la risonanza con questi risultati:distacco completo dei tendini semitendinoso bicipide femorale e del semimembranoso che appaiono retratti al terzo prossimale di coscia con travaso siero ematico fasciale a tale livello segnale osseo nella norma non evidenti lesioni delle altre strutture mio-tendinee.
volevo sapere da lei un parere su questa lesione
grazie
Salve mi scuso ho visto solo oggi il messaggio è una lesione massiva ipotizzo che abbia fatto un intervento chirurgico.